国家第八批集采181个品规将于1月13日开始报量
一、机构范围各省份公立医疗机构、军队医疗机构均应参加;其他社会办医疗机构按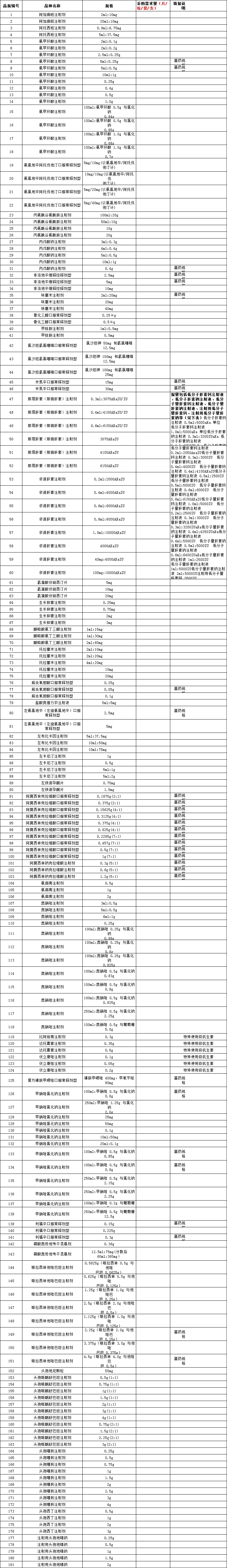
所在省份相关规定自愿参加。
二、填报方式
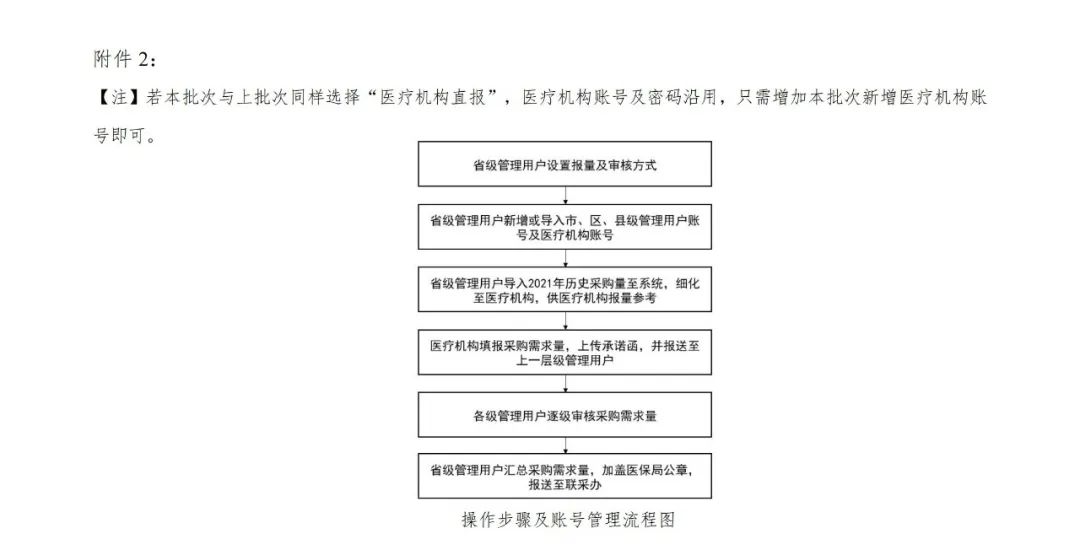
本次数据填报采用线上直报方式进行,由各省份导入2021 年历史采购量数据,供医疗机构填报相关药品采购需求量时参考,医疗机构按报量规格填报采购需求量。各省份医保部门组织辖区内相关医疗机构,在规定时间内通过"国家组织药品集中采购综合服务平台"(以下简称"系统",网址:http://blxt.smpaa.cn)完成填报工作,药品清单可在系统中查询和下载。省级管理用户账号、医疗机构账号及密码沿用第七批国家集采,具体操作方法请参照系统内操作手册或操作视频。
三、时间安排
1月12日(周四)24:00前,各省份医保部门维护管理用户账号和医疗机构账号,相关用户完成报量操作测试。
1月13日(周五)正式启动报量,各省份医保部门导入2021 年历史采购量数据供医疗机构参考。医疗机构须按要求填报相关药品采购需求量,并于2月8日(周三)24:00前提交数据。
2月21日(周二)17:00前,请各省份完成相关药品采购需求量审核工作,汇总导出并打印,加盖省医保局公章,将电子档和扫描件由系统报送至联合采购办公室。药品清单及格式见《省(区、市、兵团)相关药品采购需求量填报表》(附件1)。
填表说明
(1)口服常释剂型:普通片剂(片、素片、肠溶片、包衣片、薄膜灰片、糖衣片、浸膏片、分散片、划痕片)、硬胶囊、软胶囊(胶丸)、肠溶胶囊;不包括口腔崩解片(口崩片);(2)缓释控释剂型:缓释片、缓释包衣片、缓释胶囊、控释片、控释胶囊;(3)吸入剂:气雾剂、粉雾剂、吸入剂、吸入粉雾剂、干粉吸入剂、粉吸入剂、雾化溶液剂、吸入气雾剂、吸入(用)溶液、吸入(用)混悬液、(鼻用)喷雾剂、鼻吸入气雾剂、雾化吸入用混悬液、吸入(用)气雾剂、雾化液;(5)口服液体剂:口服溶液剂、口服混悬剂、干混悬剂、口服乳剂、胶浆剂、口服液、乳液、乳剂、胶体溶液、合剂、酊剂、滴剂、混悬滴剂、糖浆剂(含干糖浆剂);(6)注射剂:注射剂、注射液、注射用溶液剂、静脉滴注用注射液、注射用混悬液、注射液无菌粉末、静脉注射针剂、注射用乳剂、乳状注射液、粉针剂、针剂、无菌粉针、冻干粉针、注射用浓溶液;2.填写与品种名称、规格对应的采购数量;采购数量以“片/粒/袋/支”计;3. 肝素类品种报量时,请各医疗机构根据低分子肝素钠/钙等的适应症和规格使用实际,自行合理将采购需求冒归类至那曲肝素或依诺肝素报量;4. 对本次集采涉及的特殊使用级抗菌药物和基药规格,请各医疗机构分别按照《抗菌药物临床应用管理办法(卫生部令第84号)》和《关于印发国家基本药物目录管理办法的通知》(国卫药政发(2015)52号)的要求,进行合理报量。